ΣΥΜΦΥΤΙΚΗ ΘΥΛΑΚΙΤΙΔΑ
ΨΥΧΡΟΣ Ή ΠΑΓΩΜΕΝΟΣ ΏΜΟΣ
(ΑΠΟΣΠΑΣΜΑ ΑΠΟ ΤΟ ΒΙΒΛΙΟ “ΠΑΘΗΣΕΙΣ ΤΟΥ ΩΜΟΥ”, ΔΗΜ.Ι. ΓΟΥΛΕΣ, Ε.ΕΛ.Ι.Α, 2018)
ΔΡ. ΔΗΜΗΤΡΙΟΣ ΓΟΥΛΕΣ
ΡΕΥΜΑΤΟΛΟΓΟΣ – ΟΡΘΟΠΑΙΔΙΚΟΣ – ΠΑΘΟΛΟΓΟΣ
Ορισμός
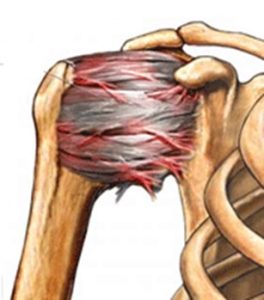
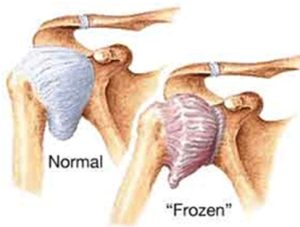
Ο παγωμένος ή ψυχρός ώμος ( frozen shoulder) ή συμφυτική θυλακίτιδα (adhesive capsulitis) επινοήθηκε και περιγράφθηκε για πρώτη φορά το 1934 από τον Codman [1]. Είναι μια επώδυνη και ποικίλης βαρύτητας νόσος που οφείλεται σε ίνωση της αρθρικής κάψας και των πέρι μορίων. Χαρακτηρίζεται από σημαντικό περιορισμό των ενεργητικών και παθητικών κινήσεων του ώμου, ιδίως της απαγωγής και της έξω στροφής, η οποία μπορεί να φτάσει μέχρι πλήρους ακινησίας του ώμου, ενώ απουσιάζουν ειδικά διαγνωστικά και απεικονιστικά ευρήματα .
Εμφανίζεται με προοδευτικό και οδυνηρό τρόπο, που οδηγεί σε ινωτική ρίκνωση της αρθρικής κάψουλας. Ο πόνος αρχικά εγκαθίσταται σταδιακά και επιτείνεται τη νύχτα [1]. Προσβάλλει άτομα μέσης ηλικίας, ιδίως τις γυναίκες. Μπορεί να είναι ιδιοπαθής ή δευτεροπαθής και εξελίσσεται σε τρία στάδια ή φάσεις : (α) επώδυνη (β) δυσκαμψίας και (γ) ανάνηψης [2].
Επιπολασμός
Είναι νόσος της μέσης ή μεγάλης ηλικίας (38-80 ετών) και οι γυναίκες προσβάλλονται συχνότερα από τους άνδρες. Η συχνότητα εμφάνισης δεν είναι ακριβώς γνωστή. Ωστόσο, εκτιμάται ότι 2 έως 5% του γενικού πληθυσμού [3] αναπτύσσει την ασθένεια αυτή κατά τη διάρκεια της ζωής του και δεν υπάρχει καμία προτίμηση για κάποια φυλή. Στους διδύμους, η συμφυτική θυλακίτιδα (ΣΘ) είναι κατά 2-3 φορές συχνότερη απ’ ό,τι στο γενικό πληθυσμό. Συνήθως η αμφοτερόπλευρη προσβολή των ώμων είναι σπάνια. Αντίθετα μπορεί να παρουσιάζεται διαδοχικά.
Η επίπτωση της συμφυτικής θυλακίτιδας του ώμου είναι πέντε φορές υψηλότερη στον διαβητικό πληθυσμό από ό,τι στο γενικό πληθυσμό, στους οποίους κυμαίνεται από 10% -29% [2,4,5]. Προσβάλλει τόσο τον τύπου 1 όσο και τον τύπου 2 ΣΔ, είναι πιο συχνή στους ηλικιωμένους, και μπορεί να είναι αμφίπλευρη [2].
Αντίστροφα, μερικοί ερευνητές μελετώντας ασθενείς με παγωμένο ώμο, ανέφεραν υψηλότερη επίπτωση εμφράγματος του μυοκαρδίου σε ασθενείς με τύπου 1 ΣΔ, και αυτόνομης νευροπάθειας σε ασθενείς με τύπου 1 και τύπου 2 ΣΔ [2].
Η πρωτοπαθής συμφυτική θυλακίτιδα του ώμου θεραπεύεται συνήθως από μόνη της μετά από 2-4 χρόνια. Μερικοί άρρωστοι έχουν συμπτώματα και περιορισμό της κινητικότητας του ώμου, ο οποίος διαρκεί πάνω από 3 χρόνια, ενώ ελάχιστοι αποκτούν μόνιμη, μακροχρόνια αναπηρία.
Αιτιολογία
Η συμφυτική θυλακίτιδα μπορεί να εκδηλωθεί χωρίς εμφανή αιτία, χωρίς σχετιζόμενη ή υποκείμενη νόσο, δηλαδή είναι άγνωστης αιτιολογίας και στην περίπτωση αυτή ονομάζεται πρωτοπαθής ή ιδιοπαθής.
Η δευτεροπαθής συμφυτική θυλακίτιδα αναπτύσσεται σε έδαφος διαφόρων νοσολογικών καταστάσεων που εμπλέκονται στο μηχανισμό της νόσου ως παράγοντες κινδύνου και αυξάνουν τη συχνότητά της , όπως:
- Σακχαρώδης διαβήτης
- Αυχενική ριζοπάθεια – μυελοπάθεια
- Μακροχρόνια ακινητοποίηση
- Κακώσεις του ώμου (τραύμα, αποτιτανώσεις, ρήξεις πετάλου, κατάγματα, χειρουργικές επεμβάσεις στον ώμο)
- Καρδιακές και νευροχειρουργικές επεμβάσεις
- Παθήσεις του θυρεοειδούς
- Εγκεφαλικά επεισόδια
- Αυτοάνοσα νοσήματα
- Νόσος Dupuytren
- Νόσος Parkinson
- Αντι-ιογενή θεραπεία (ιδιαίτερα αναστολείς της πρωτεάσης) για λοίμωξη από HIV
Οι περισσότεροι ασθενείς με ΣΘ έχουν περάσει μια περίοδο ακινητοποίησης του ώμου. Σε μια μελέτη ακινητοποιημένων ώμων (νευροχειρουργικών ασθενών) η επίπτωση παγωμένου ώμου ήταν 5 – 9 φορές μεγαλύτερη εκείνης του γενικού πληθυσμού [6].
Ιστολογία-Ανοσολογία- Παθοφυσιολογία
Η ΣΘ εμφανίζεται με προοδευτικό και οδυνηρό τρόπο, που οδηγεί σε σύγκαμψη και ρίκνωση της αρθρικής κάψουλας (contracture of the joint capsule), η οποία προσκολλάται στην κεφαλή του βραχιονίου, μειώνοντας τoν όγκο και τον διαθέσιμο λειτουργικό χώρο για τις κινήσεις της άρθρωσης [2].
Η ιστολογική εξέταση του θυλάκου δείχνει πολλαπλασιασμό των ινοβλαστών και μετατροπή τους σε μυοϊνοβλάστες, οι οποίοι παράγουν υπερβολική ποσότητα κολλαγόνου τύπου 1 και τύπου 3. Οι διαπιστώσεις αυτές είναι παρόμοιες με εκείνες της νόσου Dupuytren [7] χωρίς η ΣΘ να έχει την ίδια δυσμενή πρόγνωση.
Ενδιαφέρον είναι ότι εκτός από την γληνοβραχιόνια κάψα συχνά εμπλέκονται στην απώλεια εύρους κίνησης βλάβες των περιαρθρικών δομών, όπως ο κορακοβραχιόνιος σύνδεσμος, το στροφικό πέταλο, ο υποπλάτιος μυς και ο υπακρωμιακός ορογόνος θύλακας. Περίεργο είναι ότι οι περισσότεροι συγγραφείς δεν περιγράφουν κλινικά σοβαρές συμφύσεις της κάψας ως κυρίαρχο εύρημα της χρόνιας θυλακίτιδας. Αντίθετα, επιβεβαιώνουν μια ενεργή υπερπλαστική ινοπλασία και υπέρμετρη παραγωγή κολλαγόνου τύπου ΙΙΙ που οδηγεί σε συγκάμψεις των προαναφερθέντων μαλακών ιστών. Τα ευρήματα αυτά παρατηρήθηκαν σε χειρουργημένους ασθενείς τελικού σταδίου και δεν μπορούν να βρεθούν σε ασθενείς πρώιμου σταδίου. Παρά τις ιστολογικές ομοιότητες με τις συσπάσεις Dupuytren, η ΣΘ διαφέρει από τη δυσμενή, και προοδευτική έκβαση της πρώτης. Οι παραπάνω βλάβες οδηγούν σε προοδευτική απώλεια εύρους κίνησης της γληνοβραχιόνιας άρθρωσης, η οποία επηρεάζει την έξω στροφή και απαγωγή, έπειτα την κάμψη, την προσαγωγή και την έκταση με καθοδική σειρά σοβαρότητας.
Ο ρόλος της φλεγμονής και ανοσολογίας.
Ανοσολογικές, φλεγμονώδεις και ινώδεις αλλοιώσεις φαίνεται να εμπλέκονται στην παθοφυσιολογία της ΣΘ [8]. Η τρέχουσα υπόθεση ξεκινά με την εμφάνιση φλεγμονής στον αρθρικό θύλακο [9]. Πιθανώς η φλεγμονή αρχίζει μέσα και γύρω από την μασχαλιαία πτυχή του θυλάκου και ακολουθείται από δημιουργία συμφύσεων και ίνωση του υμενικού επιθηλίου και της κάψας, η οποία παχαίνει και συρρικνώνεται [10].
Οι βιοδείκτες του αρθρικού υγρού υποδηλώνουν την παρουσία χρόνιας φλεγμονής [11]. Οι παρακάτω βιοδείκτες έχουν εντοπιστεί [12, 13]:
- Διακυττάριο μόριο συγκόλλησης – 1 (ICAM-1, CD54)
- Αυξητικός παράγοντας μετασχηματισμού-β (TGF-β)
- Παράγοντας νέκρωσης των όγκων-άλφα (TNF-α)
- Ιντερλευκίνη-1 (IL-1) άλφα και βήτα
- IL-6
- Αιμοπεταλιακός αυξητικός παράγοντας (PDGF)
Τα ένζυμα οι μεσοκυττάριες μεταλλοπρωτεϊνάσες εμπλέκονται στην κατασκευή του εξωκυττάριου συνδετικού ιστού (extracellular matrix) και στις διάφορες κυτταροκίνες που ελέγχουν την εναπόθεση κολλαγόνου. Τα φάρμακα που αναστέλλουν τις μεσοκυττάριες μεταλλοπρωτεϊνάσες μπορεί να προκαλέσουν συνθήκες πολύ παρόμοιες με τη ΣΘ και τη νόσο Dupuytren [3].
Μικροαγγειακές παθήσεις όπως ο σακχαρώδης διαβήτης μπορεί να προκαλέσουν μη φυσιολογική επιδιόρθωση κολλαγόνου, η οποία προδιαθέτει τους ασθενείς για ανάπτυξη ΣΘ [14].
Η νεοαγγείωση με χρώση του αγγειακού ενδοθηλιακού αυξητικού παράγοντα (VEGF) έχει επίσης εντοπιστεί σε ιστικά δείγματα διαβητικών ασθενών [3]. Η αυξημένη γλυκοζυλίωση της πρωτεΐνης κολλαγόνου, ο αυξημένος σχηματισμός μη φυσιολογικών τελικών προϊόντων γλυκοζυλίωσης και η μετέπειτα συσσώρευσή τους έχουν δυσμενή επίδραση στις κυτταρικές και εξωκυττάριες διεργασίες οι οποίες ενδέχεται να διευκολύνουν την ίνωση και τις συμφυτικες διαδικασίες [15].
Συμπερασματικά μετά τη φλεγμονώδη διαδικασία του αρθρικού υμένα, εμφανίζεται ένας μεγάλος αριθμός ινοβλαστών και μυοϊνοβλαστών, με παράλληλη παρουσία δεικτών φλεγμονής, ενώ ένζυμα (μεταλλοπρωτεϊνάσες), μικροαγγειοπάθεια νεοαγγειογένεση και αυξημένη γλυκοζυλίωση του κολλαγόνου διαταράσσουν την παραγωγή του. Όλοι αυτοί οι παράγοντες προάγουν έντονα την ινωτική διεργασία, πάχυνση και ρίκνωση του αρθρικού θυλάκου προκαλώντας κλινικά πόνο και δυσκαμψία [13,16].
Κλινική εικόνα
Τυπικά, ο άρρωστος με συμφυτική θυλακίτιδα έχει μια ποικιλία επώδυνων συμπτωμάτων και δυσκαμψίας του ώμου που συνήθως επιδεινώνονται κατά τη διάρκεια της νύχτας εμποδίζοντας τον ύπνο ιδίως στην ομόπλευρη κατάκλιση. Η όλη κατάσταση δυσκολεύει τον ασθενή στις καθημερινές, επαγγελματικές και αθλητικές του δραστηριότητες.
Τα συμπτώματα εξελίσσονται διαχρονικά και διαβαθμίζονται από ασθενή σε ασθενή από ήπια έως έντονα και αναπηρικά. Έχει επικρατήσει η νόσος να διαχωρίζεται σε 3 στάδια (φάσεις), αν και υπάρχουν κατά την γνώμη μας επικαλύψεις και ασάφεια στην προτεινόμενη σταδιοποίηση:
1η φάση: επώδυνη (freezing, παγωμένη) φάση
Οι ασθενείς αρχικά έχουν πόνο με τις δραστηριότητες τον οποίο συχνά αποδίδουν σε ήπιες κακώσεις και δυσκαμψία η οποία προοδευτικά επιδεινώνεται. Ο πόνος είναι διάχυτος, έντονος έως δραματικός δυσκολεύοντας τον ύπνο.
Συνήθως εμφανίζεται πριν από τον περιορισμό της κινητικότητας, αν και, σε μερικές περιπτώσεις, ο άρρωστος παρουσιάζεται με κατάργηση της κινητικότητας του ώμου. Η φάση αυτή διαρκεί 10-36 εβδομάδες.
2η φάση: Δύσκαμπτη ή « κατεψυγμένη» (frozen) φάση
Η «παγωμένη» φάση ακολουθείται από την δύσκαμπτη ή «κατεψυγμένη» φάση, στην οποία ο πόνος προοδευτικά μειώνεται αλλά ο άρρωστος συνεχίζει να έχει δυσκαμψία και σοβαρό περιορισμό της κινητικότητας του ώμου. Η φάση αυτή διαρκεί 4-12 μήνες.
 3η φάση: Φάση αποκατάστασης ή απόψυξης («thawing»)
3η φάση: Φάση αποκατάστασης ή απόψυξης («thawing»)
Στην φάση αυτή (η οποία διαρκεί 5-24 μήνες), προοδευτικά, η κινητικότητα και λειτουργικότητα του ώμου βελτιώνεται αυτόματα, δηλ. ο ώμος «ξεπαγώνει» από μόνος του.
ΚΛΙΝΙΚΑ ΔΕΔΟΜΕΝΑ
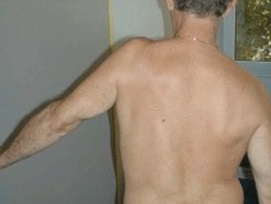
Οι ασθενείς δυσκολεύονται ή αδυνατούν να φορέσουν το σακάκι, το πουκάμισο, το στηθόδεσμο (σουτιέν) ή να χτενισθούν, να φέρουν το χέρι τους πίσω από το κεφάλι, ή να βάλουν τα βιβλία στα ψηλά ράφια της βιβλιοθήκης. Κατά την κλινική εξέταση σε σύγκριση με τον υγιή ώμο οι ασθενείς παρουσιάζουν επώδυνη και σημαντική μείωση των ενεργητικών και παθητικών κινήσεων του ώμου σε πολλά επίπεδα (συνήθως της απαγωγής, της ανύψωσης και της έξω στροφής).
Οι Pal και συν [17] έχουν προτείνει κλινικά κριτήρια για τη διάγνωση της συμφυτικής θυλακίτιδας του ώμου που περιλαμβάνουν: 1) πόνο στον ώμο για τουλάχιστον ένα μήνα, 2) περιορισμό της ενεργητικής και παθητικής κινητικότητας σε τουλάχιστον τρία επίπεδα, 3)αδυναμία ωμόπλευρης κατάκλισης στον ώμο.
Διάγνωση και Διαφορική διάγνωση
Δεν υπάρχουν εργαστηριακά ή απεικονιστικά ευρήματα διαγνωστικά της συμφυτικής θυλακίτιδας. Η διάγνωση του «παγωμένου» ώμου γίνεται κλινικά με βάση το ιατρικό ιστορικό και την κλινική εξέταση, αφού αποκλεισθούν ο διαβήτης και άλλα νοσήματα που εμπλέκονται με παγωμένο ώμο που ήδη αναφέρθηκαν παραπάνω.
Παρόμοια συμπτωματολογία της θυλακίτιδας μπορεί να προκαλέσουν και άλλες καταστάσεις ή παθήσεις, όπως οι ρήξεις του στροφικού πετάλου, η ασβεστοποιός τενοντίτιδα, η τενοντοελυτρίτιδα του δικεφάλου βραχιονίου, η αρθρίτιδα της γληνοβραχιόνιας και της ακρωμιοκλειδικής.
Οι καταστάσεις αυτές μπορεί να προκαλέσουν φανερό περιορισμό του ενεργητικού εύρους κίνησης του ώμου, αλλά δεν προκαλούν πραγματική σύγκαμψη του θυλάκου και περιορισμό των παθητικών κινήσεων του ώμου.
Κλινικά, είναι εύκολο να ξεχωρίσουμε την συμφυτική θυλακίτιδα από την οστεοαρθρίτιδα του ώμου ή την αρθρίτιδα του ώμου σε έναν άρρωστο με ρευματοειδή αρθρίτιδα. Η διάγνωση και διάκριση μεταξύ των καταστάσεων αυτών (προσβολή του ώμου στην οστεοαρθρίτιδα, την ρευματοειδή αρθρίτιδα και την συμφυτική θυλακίτιδα) διευκολύνεται με απεικονιστικές μεθόδους, και την κλινικοεργαστηριακή εκτίμηση.
Άλλες καταστάσεις που μοιάζουν με «παγωμένο» ώμο
- Αναφερόμενος πόνος από τον αυχένα ή το διάφραγμα
- Εκφυλιστική δισκαρθροπάθεια ΑΜΣΣ
- Ρευματική πολυμυαλγία*
- Κακοήθη νοσήματα (ιδιαίτερα μεταστάσεις και καρκίνος της κορυφής του πνεύμονα)
- Σύνδρομο θωρακικής εξόδου
- Σύνδρομο υπερπλατίου νεύρου
Ένεση στον υπακρωμιακό χώρο
Για την δδ της ΣΘ από υπακρωμιακές τενοντοπάθειες κάνουμε μια ένεση με αναισθητικό στον υπακρωμιακό χώρο. Σε ασθενείς με συμφυτική θυλακίτιδα η ένεση δεν βελτιώνει το εύρος κίνησης και τον πόνο. Στους ασθενείς όμως με πόνο οφειλόμενο σε παθήσεις του υπακρωμιακού χώρου (π.χ. τενοντοπάθεια στροφικού πετάλου, υπακρωμιακή θυλακίτιδα) ανακουφίζει γενικά από τον πόνο και βελτιώνει το εύρος κίνησης.
ΑΠΕΙΚΟΝΙΣΤΙΚΑ
Δεν βοηθούν ιδιαίτερα στη ουσιαστική διάγνωση της νόσου, η οποία τίθεται συνήθως με ευχέρεια με την κλινική εξέταση από τον έμπειρο κλινικό. Μερικές φορές επιβάλλεται να αποκλεισθούν απεικονιστικά άλλα νοσήματα που μιμούνται τη νόσο όπως η οστεονέκρωση, το λανθάνον κάταγμα, η ρήξη του πετάλου, η οστεοαρθρίτιδα κ.α.
Απλές ακτινογραφίες
Οι απλές ακτινογραφίες εκτός από πιθανή οστεοπενία συνήθως δεν δείχνουν τίποτα το παθολογικό, αλλά συμβάλουν στον αποκλεισμό άλλων νοσημάτων όπως: λανθάνον κάταγμα, οστεοαρθρίτιδα και οστεονέκρωση (όψιμα).
Μαγνητική τομογραφία
Εάν ο άρρωστος έχει τυπικό ιστορικό και κλινικά ευρήματα, η MRI δεν χρειάζεται, εφ’ όσον έχουμε αποκλείσει άλλες νοσολογικές καταστάσεις.
Η MRI με ή χωρίς σκιαγραφικό ή το MRI αρθρογράφημα, μπορεί να αναδείξει έμμεσα ευρήματα όπως η πάχυνση του αρθρικού θυλάκου και του κορακοβραχιόνιου συνδέσμου ή πάχυνση του θυλάκου της μασχαλιαίας πτυχής και ελάττωση του ενδοκαψικού ζωτικού χώρου από τη ρίκνωση του θυλάκου.
Το υπερηχογράφημα μπορεί να βοηθήσει στη διάγνωση της συμφυτικής θυλακίτιδας και να αποκλείσει παθολογικές καταστάσεις του στροφικού πετάλου και του αρθρικού θυλάκου του ώμου.
ΘΕΡΑΠΕΙΑ
Δεν υπάρχει ομοφωνία για το ποια είναι η καλύτερη θεραπεία του «παγωμένου» ώμου. Η θεραπεία απαιτεί πείρα, χρόνο και δεν είναι εύκολη υπόθεση. Υπάρχουν πολλοί τρόποι και μέθοδοι να «θεραπεύσει» κανείς τον «παγωμένο» ώμο. Δεν υπάρχει όμως ομοφωνία. Πολλές ειδικότητες ασχολούνται με την θεραπεία, όπως οι φυσιοθεραπευτές , φυσίατροι, ρευματολόγοι, ορθοπεδικοί. Συνοπτικά η θεραπεία αποτελείται από αναλγητικά και ΜΣΑΦ, φυσιοθεραπεία, διηθήσεις με κορτικοστεροειδή, οστεοπαθητικούς χειρισμούς και χειρισμούς υπό αναισθησία, και αρθροσκοπική απελευθέρωση. Οι περισσότεροι ασθενείς ανακτούν κανονική λειτουργικότητα – κινητικότητα [18].
Στην φάση σύμφυσης (adhesive phase), η απελευθέρωση της κάψουλας μπορεί να πραγματοποιηθεί μέσω ήπιων χειρισμών (manipulation) υπό αναισθησία ή χειρουργικώς [2,18]. Με αυτό το τρόπο βίαια σπάζουν οι συμφύσεις και επανέρχεται η κίνηση. Το μειονέκτημα αυτής της μεθόδου είναι η πιθανότητα κατάγματος στη περιοχή του ώμου , κυρίως σε ηλικιωμένους ασθενείς.
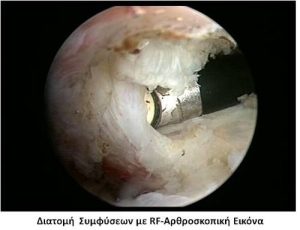
Νεότερες αντιλήψεις συστήνουν την αρθροσκοπική διατομή του αρθρικού θύλακα και λύση των συμφύσεων στο υπακρωμιακό χώρο. Το πλεονέκτημα αυτής της μεθόδου είναι η ελεγχόμενη διατομή με αποφυγή δημιουργίας κατάγματος. Τα αποτελέσματα είναι αρκετά καλά. Μειονέκτημα είναι η ανάγκη αρθροσκοπικής επέμβασης.
Η μετεγχειρητική πορεία του ασθενούς είναι σχετικά εύκολη. Τοποθετείται ανάρτηση του άνω άκρου για μερικές μέρες για ανακούφιση των συμπτωμάτων. Ταυτόχρονα αρχίζει η κινητοποίηση του ώμου (φυσιοθεραπεία) με στόχο την αποκατάσταση του εύρους κινήσεων του ώμου. Αργότερα προστίθεται και η ενδυνάμωση των μυών.
Η χειρουργική απελευθέρωση πραγματοποιείται κατά προτίμηση μέσω της αρθροσκόπησης και όχι με ανοικτή χειρουργική επέμβαση, επειδή με τον πρώτο τρόπο μειώνεται η μετεγχειρητική περίοδος ανάρρωσης [2,19].
Αρχική εκτίμηση
- Καλό ιστορικό και σωστή και προσεκτική κλινική εξέταση
- Απλές ακτινογραφίες για να αποκλείσετε άλλες καταστάσεις
- Υπερηχογράφημα ή MRI για να αποκλείσετε παθήσεις του στροφικού πετά λου
- Εάν δυσκολεύεστε να βάλετε διάγνωση, κάντε μίαν ένεση κορτιζόνης μαζί με αναισθητικό (π.χ. 20-40 mg ακετονικής τριαμσινολόνης μαζί με 5 mL λιδοκαΐνης 1%) μέσα στη γληνοβραχιόνια άρθρωση
Συντηρητικές θεραπείες
Ένα παυσίπονο, π.χ. ακεταμινοφαίνη. Συνδυάστε το και με ένα μη στεροειδές αντιφλεγμονώδες. Στα αρχικά στάδια της νόσου μπορείτε να δώσετε οπιοειδή αναλγητικά.
Ο άρρωστος μπορεί ακόμα να ανακουφισθεί από τον πόνο και να βελτιώσει την κινητικότητα του ώμου με κορτιζόνη από το στόμα, π.χ. 30 mg πρεδνιζολόνης καθημερινά 3 φορές την εβδομάδα.
Εάν ο άρρωστος έχει μέτρια έως σοβαρά συμπτώματα, η ενδαρθρική ένεση κορτιζόνης ή η ενδαρθρική διάταση της άρθρωσης είναι ωφέλιμη. Μια ή περισσότερες ενέσεις κορτιζόνης στον ώμο μπορεί να ανακουφίσει τον άρρωστό και να βελτιώσoυν την κινητικότητα του ώμου για πολλούς μήνες.
Τους επόμενους μήνες :
- Ανάπαυση του ώμου σε συνδυασμό με ήπιες ασκήσεις εύρους κίνησης της γληνοβραχιόνιας άρθρωσης.
- Εάν ο άρρωστος έχει μικρή βελτίωση ή δεν ανταποκρίνεται στη θεραπεία στη διάρκεια της παρακολούθησης (περίπου κάθε 3-4 εβδομάδες) : ενδαρθρική ένεση κορτιζόνης και ασκήσεις στο σπίτι.
- Εάν η κατάσταση είναι βελτιωμένη στις επόμενες επισκέψεις: περισσότερο επιθετικές ασκήσεις, για να αυξηθεί το εύρος κίνησης.
- Περιοδική (κάθε 2-3 μήνες) επανεκτίμηση του εύρους κίνησης του ώμου.
- Οι ασθενείς μπορούν να κάνουν περισσότερο εντατικές ασκήσεις στο σπίτι καλύτερα με φυσιοθεραπευτή.
Χειρουργική επέμβαση
Η χειρουργική επέμβαση φαίνεται ότι δεν βελτιώνει την πρόγνωση, γι’ αυτό και επιφυλάσσεται για ασθενείς που δεν ανταποκρίνονται στη συντηρητική αγωγή.
Συμπερασματική άποψη των συγγραφέων
Η ΣΘ είναι μια επώδυνη νόσος ποικίλης βαρύτητας. Σύμφωνα με την πείρα μας η θεραπευτική παρέμβαση με ΜΣΑΦ, 3-6 τοπικές εγχύσεις κορτικοστεροειδών και φυσικοθεραπεία με διατατικές ασκήσεις λύνουν το επώδυνο σύνδρομο σε 2 εβδομάδες περίπου και σε 4-8 εβδομάδες αποκαθιστούν λειτουργικά τον ασθενή στο 95% των περιπτώσεων χωρίς καμιά επιπλοκή. Οι διαβητικοί ανταποκρίνονται με βραδύτερους ρυθμούς, χρειάζονται περισσότερη φυσικοθεραπεία και λιγότερη δοσολογία φαρμάκων ,ιδίως των ΜΣΑΦ τα οποία επιβαρύνουν δυνητικά τα νεφρά.
ΒΙΒΛΙΟΓΡΑΦΙΑ
- Lebiedz-Odrobina D, Kay J. Rheumatic manifestation of diabetes mellitus. Rheum Dis Clin N Am 2010;36(4):681-99.
- Binder AI, Bulgen DY, Hazleman BL, Roberts S. Frozen shoulder: a long-term prospective study. Ann Rheum Dis. 1984 Jun. 43(3):361-4.
- Hsu JE, Anakwenze OA, Warrender WJ, Abboud JA. Current review of adhesive capsulitis. J Shoulder Elbow Surg. 2011 Apr. 20(3):502-14.
- Song KD, Kwon JW, Yoon YC, Choi SH. Indirect MR Arthrographic Findings of Adhesive Capsulitis. AJR Am J Roentgenol. 2011 Dec. 197(6):W1105-9.
- Carbone S, Napoli A, Gumina S. MRI of adhesive capsulitis of the shoulder: Distension of the bursa in the superior subscapularis recess is a suggestive sign of the pathology. Eur J Radiol. 2013 Oct 29.
- Bruckner FE, Nye CJ. A prospective study of adhesive capsulitis of the shoulder (“frozen shoulder”) in a high risk population. Q J Med. 1981 Spring. 50(198):191-204.
- Bunker TD, Anthony PP. The pathology of frozen shoulder. A Dupuytren-like disease. J Bone Joint Surg Br 1995;77(5):677-83.
- Ryan V, Brown H, Minns Lowe CJ, Lewis JS. The pathophysiology associated with primary (idiopathic) frozen shoulder: A systematic review. BMC Musculoskelet Disord. 2016 Aug 15. 17(1):340.
- Ozaki J, Nakagawa Y, Sakurai G, et al. Recalcitrant chronic adhesive capsulitis of the shoulder. Role of contracture of the coracohumeral ligament and rotator interval in pathogenesis and treatment. J Bone Joint Surg Am. 1989 Dec. 71(10):1511-5.
- Neviaser AS, Hannafin JA. Adhesive Capsulitis: A Review of Current Treatment. Am J Sports Med. 2010 Jan 28, 215-31.
- Kim YS, Kim JM, Lee YG, Hong OK, Kwon HS, Ji JH. Intercellular adhesion molecule-1 (ICAM-1, CD54) is increased in adhesive capsulitis. J Bone Joint Surg Am. 2013 Feb 20. 95(4):e181-8.
- Rodeo SA, Hannafin JA, Tom J, Warren RF, Wickiewicz TL. Immunolocalization of cytokines and their receptors in adhesive capsulitis of the shoulder. J Orthop Res. 1997 May. q5(3):427-36.
- Song A, Higgins LD, Newman J, Jain NB. Glenohumeral corticosteroid injections in adhesive capsulitis: a systematic search and review. PM R. 2014 Dec. 6(12):1143-56.
- Siegel LB, Cohen NJ, Gall EP. Adhesive capsulitis: a sticky issue. Am Fam Physician. 1999 Apr. 59(7):1843-52.
- Thomas SJ, McDougall C, Brown ID, Jaberoo MC, Stearns A, Ashraf R, et al. Prevalence of symptoms and signs of shoulder problems in people with diabetes mellitus. J Shoulder Elbow Surg. 2007 Nov-Dec. 16(6):748-51.
- Uppal HS, Evans JP, Smith C. Frozen shoulder: A systematic review of therapeutic options. World J Orthop. 2015 Mar 18. 6(2):263-8.
- Pal B, Anderson J, Dick WC, Griffiths ID. Limitation of joint mobility and shoulder capsulitis in insulin- and non-insulin-dependent diabetes mellitus. Br J Rheumatol 1986;25 (2):147-51.
- Lloyd-Roberts GC, French PR. Periarthritis of the shoulder. A study of the disease and its treatment. Br Med J. 1959. 1:1569-71.
- Chi AS, Kim J, Long SS, Morrison WB, Zoga AC. Non-contrast MRI diagnosis of adhes.capsulitis of the shoulder. Clin Imaging. 2017 Apr 7. 44:46-50.